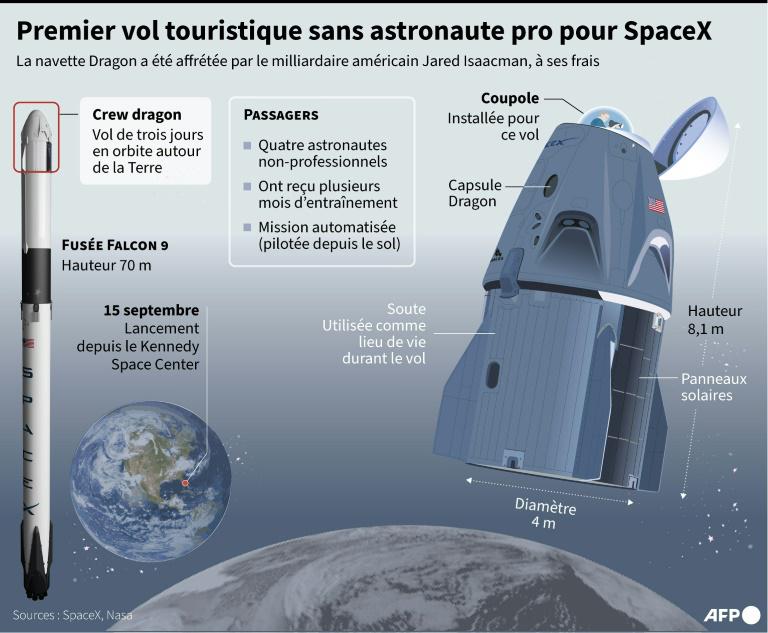
Vaccin Astrazeneca : efficacité, méthode, effets secondaires
Le vaccin Astrazeneca est autorisé en France uniquement pour les plus de 55 ans. Un risque thrombose ayant été confirmé en dessous de cet âge. Selon l'agence européenne du médicament, 833 cas de syndrome de Guillain Barré ont également été rapportés dans le monde après une injection de Vaxzevria.
- Est-il moins bon que Pfizer et Moderna ?
- Prix et conservation
- Comment fonctionne-t-il ?
- Sa composition
- Quel délai entre les 2 doses ?
- Quelle efficacité ?
- Vaccin Astrazeneca : pour qui ?
- Efficacité contre les variants
- Des contre-indications
- Liste des effets secondaires
- Comment réagir en cas d'effets secondaires ?
- Que faire si j'ai moins de 55 ans et j'ai été vacciné par Astrazeneca ?
- Le retard de livraison des doses en France
Dernières actualités concernant le vaccin AstraZeneca :
Le vaccin Astrazeneca anti covid a subi de nombreuses critiques et rebondissements à cause de la déclaration d'effets secondaires après le début de son utilisation dans l'arsenal vaccinal européen, notamment quelques cas de caillots sanguins pouvant entraîner une thrombose et des décès chez des personnes vaccinées.
Comme de nombreux pays, la France avait suspendu à partir du 15 mars l'utilisation du vaccin Astrazeneca suite aux premiers signalements de thrombose. L'EMA a doncdû ré-évaluer le vaccin, mais confirme que ce ne sont que de "rares" cas. La balance bénéfice/risque reste avantageuse et le vaccin "sûr et efficace", selon eux. Ayant suivi cet avis, ainsi que l'analyse de la HAS (autorité sanitaire française), la France a de nouveau autorisé l'utilisation du sérum, mais ce dernier recommandé uniquement pour les personnes âgées de plus de 55 ans, les risques de caillots ayant été principalement constatés chez les patients en dessous de cette tranche d'âge.
Certains pays comme le Danemark ont pris la décision d'arrêter son utilisation. La Norvège est aussi entrain de réfléchir à suivre cet exemple.
Toutes les nouvelles livraisons de vaccins AstraZeneca prévues pour la France seront désormais basculées vers les dons aux pays en développement, d'après l'annonce du ministère de la Santé mardi 20 juillet. "Environ 1 million de doses d'AstraZeneca" doivent d'ailleurs être livrées cette semaine. Elles seront "100% fléchées à Covax", le dispositif de solidarité internationale, a informé un représentant du ministère de l'Economie et des Finances lors d'un point presse en ligne.Le vaccin d'AstraZeneca connait une désaffection en France à cause de ses effets secondaires. Depuis avril l'Hexagone a "cédé près de 5 millions de doses via Covax".
Effets secondaires, efficacité, composition...On fait le point sur ce que vous devez savoir si vous allez vous faire vacciner par le vaccin Astrazeneca.
Est-il moins bon que Pfizer et Moderna ?
Après les annonces des résultats de l’alliance Pfizer/BioNTech et celui de Moderna vantant une efficacité de 90% pour le premier et 94,5% pour le second (données basées sur les communiqués des laboratoires, sans publication dans aucune revue scientifique pour l’instant), AstraZeneca présente des résultats moins impressionnants, mais avec publication détaillée dans une revue scientifique.
Engagé dans la course au vaccin contre le Covid-19, le laboratoire AstraZeneca avait annoncé dans un communiqué signé en collaboration avec l’université d’Oxford, une efficacité en moyenne estimée à 70% pour son vaccin en phase clinique III (dernière phase avant demande commercialisation). Des résultats intermédiaires obtenus suite à des essais cliniques menés à grande échelle au Royaume-Uni et au Brésil. Il est le premier vaccin dans la liste des candidats dont le niveau d'efficacité a été confirmée, mardi 8 décembre, par la revue The Lancet.
Une récente étude américaine, publiée par le laboratoire Astrazeneca, effectuée à plus large échelle et situation réelle de vaccination auprès de la population américaine a revu l'efficacité à hauteur de 80%.
Prix et conservation
Le vaccin Astrazeneca est moins coûteux que ceux de Pfizer et BionTech (environ 2,50 euros la dose) et plus simple à stocker car il n’a pas besoin d’être conservé à une température très basse.
Il peut en effet être conservé à la température d'un réfrigérateur classique, soit entre 2 et 8° Celsius, à la différence des vaccins de Moderna et de Pfizer/BioNTech. Ces derniers ne peuvent être stockés à long terme qu'à très basse température (-20° Celsius pour le premier, -70°C pour le second), ne facilitant pas une vaccination à grande échelle.
Dans ses recommandations la HAS a également confirmé que pharmaciens et sages-femmes pourraient participer à la vaccination avec le vaccin Astrazneca étant donné sa facilité de conservation.
Comment fonctionne-t-il ?
À la différence des vaccins Pfizer et Moderna qui utilisent tous les deux une technologie innovante dites "ARN messager" encore jamais approuvée sur l’homme à ce jour, le vaccin d’AstraZeneca a recours à un procédé traditionnel, à vecteur viral appelé "Covid Shield".
À voir aussiArticleLa chimiothérapie et ses effets secondaires
ArticlePhytostérols : quels sont les effets secondaires ?
Baptisé ChAdOx1, lors des phases I et II, puis AZD1222 en phase III, le vaccin Astrazeneca/Oxford est composé d’un adénovirus de chimpanzé (famille de virus qui se transmet par voie féco-orale), modifié pour être inoffensif pour l’homme. “Nous avons préféré choisir un adénovirus de singe afin que le corps humain n’y ait pas déjà développé une réponse immunitaire”, explique Helen McShane, directrice du Centre de recherche biomédicale d’Oxford (BRC). Dans le génome de ce virus, les scientifiques y ont injectéun bout d'ADN du coronavirus Sars-COv 2 quipermet de reproduire la protéine Spike. Elle est identifiée comme étant la clé qui permet au virus de s’introduire dans les cellules humaines. Ce procédé permet 'entraîner une réaction immunitaire à la fois par la production d'anticorps et par la mise en oeuvre d'une fonction de mémoire de certaines cellules permettant l'activation des défense en cas d'attaque.
Sa composition
Le vaccin Astrazeneca contient sur une dose de 0,5 ml :
Des excipients :
Quel délai entre les 2 doses ?
Le vaccin Astrazeneca contre la Covid-19 est administré par injection intra-musculaire en deux doses. La deuxième devant être faite entre 9 et 12 semaines après la première, selon les recommandations de la HAS lors de la conférence de presse du 2 février 2021.
Selon le Pr Elisabeth Bouvet, membre de la commission techniques des vaccins à la HAS, des études sont à venir en vue de conseillerl'administration d'une seule dose pour les personnes ayant déjà eu la Covid-19. Des résultatsauraient montré que les personnes ayant déjà été touchées par le coronavirus aurait obtenu la même efficacité dès la première dose que ceux en ayant reçu deux. Plus de recherches doivent confirmer cette mémoire immunitaire possible.
Quelle efficacité ?
Une étude clinique de phase III récente menée aux Etats-Unis, publiée par le laboratoire Astrazeneca rapporte une efficacité, plus élevée que les premières études de grande ampleur. Menée sur plus de 32 000 personnes ayant reçu les deux doses de vaccin avec 4 semaines d'écart, l'étude comprend 60% de patients avec des comorbidités, donc à risque et 20% d'entre-eux ont plus de 65 ans. Les conclusions dont :
Des données concernant les plus de 65 ans qui jusque là manquait à l'appel et avait conduit à ne le recommander pour les plus âgés que bien plus tard.
Une efficacité à 90 % avec une demi dose et 62 % avec une dose entière
Le vaccin AstraZeneca repose sur deux injections à un mois d'écart. Lors de la phase II, le vaccin Astrazeneca/Oxford avait été testé sur 560 volontaires. Selon la deuxième étude préliminaire clinique publiée par AstraZeneca et l’université d’Oxford, le 23 novembre, dans la revue médicale The Lancet, le vaccin a été testé sur près de 13 000 volontaires et a obtenu une moyenne d'efficacité de 70%. Des résultats validées ensuite par la revue scientifique le 8 décembre.
Mais depuis leur publication, ces résultats posent problème. Le vaccin a d’abord montré une efficacité de 90% sur un premier échantillon de 3 000 personnes puis cette efficacité est descendue à 62 % lors d’un nouveau test chez un autre groupe de près de 9 000 volontaires.
Les explications révélées dans un articles de la BBC, expliquent que dans le premier groupe où le vaccin a été efficace à 90%, les volontaires ont reçu, par erreur, une demi dose seulement en premier, puis une dose entière un mois plus tard. Et dans le groupe qui a obtenu 62%, les volontaires ont reçu leurs deux injections chacun avec la dose entière.
Une plus grande efficacité obtenue donc, par erreur, sur laquelle le laboratoire a annoncé devoir se pencher afin de comprendre pourquoi avec une demi dose sur les deux injections, la réponse immunitaire a été la plus forte.
C’est donc sur cet écart d’efficacité entre les deux tests que le laboratoire doit se pencher.
Lors d’une conférence de presse, Andrew Pollard, professeur à l’université d’Oxford a expliqué que l’hypothèse principale est qu’une dose plus petite du vaccin, puis une autre plus grande par la suite permettrait une meilleure imitation de l'intrusion du virus dans l'organisme et donc une meilleure réaction du système immunitaire pour se défendre.
Selon les résultats publiés dans The Lancet, la réponse immunitaire est la même chez les sujets jeunes et âgés. Un point positif car "les adultes les plus âgés ont un risque décuplé de faire une forme grave de Covid-19, et il est donc essentiel qu'un vaccin destiné à lutter contre cette maladie soit efficace dans ce groupe de population", commentent les scientifiques. Mais une limite à cet avantage a été ajoutée dans l’étude, car parmi les volontaires, les plus vieux avaient 74 ans et étaient en bonne santé. Cela ne constitue pas un échantillon suffisamment représentatif de la population senior. Plus de recherches doivent être menées sur ce point pour élargir les données à des personnes avec des problèmes de santé et donc plus à risque encore de forme grave de Covid-19.
Vaccin Astrazeneca : pour qui ?
Les recommandations du vaccin Astrazeneca font l'affaire d'un véritable casse tête avec des rebondissements continus depuis sont autorisation. La dernière mise à jour en date de la HAS, le vendredi 19 mars recommande le vaccin, uniquement pour les plus de 55 ans, en raison d'un risque de thrombose possiblement identifié en dessous de cet âge, à la suite de nombreux signalements de cas.
Avant cela : lors de la conférence de presse du 2 février, le Pr Elisabeth Bouvet de la HAS avait expliqué que le vaccin Astrazeneca n'était pas recommandé pour les personnes âgées de plus de 65 ans à cause d'un manque de données. La majorité des études fournies à la validation du vaccin portaient principalement sur les personnes âgées entre 18 et 65 ans et les moins de 65 ans, permettant de confirmer une efficacité pour ces catégories de personnes. Plus d'études ensuite été fournis et le 2 mars 2021, la HAS annonçait dans un communiqué qu'une étude écossaise en vie réelle "soumise au British Medical Journal et en attente de revue par les pairs, apportent des résultats très encourageants sur les bénéfices à court terme d’une première dose de vaccin (Pfizer ou AstraZeneca) contre la Covid-19 chez les plus de 65 ans." Dans cette étude l'impact du vaccin a été analysé sur 5 millions d'habitants en Ecosse. Parmi les tranches d'âges étudiées : les 18-64 ans, 65-70 ans et les plus de 80 ans. La baisse du risque d'hospitalisation a été bénéfique à toutes les tranches d'âges selon la HAS. "Les effets les plus marqués sont observés de 28 à 34 jours après la première injection : efficacité de 85% pour les 18-64 ans, 79% pour les 65-79 ans et 81% pour les plus de 80 ans." En conséquence, la HAS avait redéfinit la place du vaccin AstraZeneca dans la stratégie vaccinale en élargissant son utilisation aux personnes âgées de plus de 65 ans.
NEW #guide by @ethical_net | How to Eat a Planet-Friendly Diet 🤔⬇️⬇️⬇️🍽️🌍 #foodsystem #carbonfootprint #organic… https://t.co/cPkSt1oy5R
— ethical.net Sat Aug 03 15:21:15 +0000 2019
Par manque de données également, le vaccin n'est toujours pas recommandé aux femmes enceintes, ni aux personnes immunodéprimées.
Efficacité contre les variants
Variant anglais
Une étude préliminaire publiée menée sur des volontaires vaccinés entre le 1er octobre 2020 et le 14 janvier 2021 (date de la flambée du variant anglais au Royaume-Uni) par la Oxford University a montré que le vaccin Astrazeneca était efficace contre le variant britannique B.1.1.7.
Selon le directeur général d'AstraZeneca Pascal Soriot interviewé par le Sunday Times sur le variant britannique, "nous pensons pour l'instant que le vaccin devrait rester efficace. Mais on ne peut pas en être sûr donc nous allons faire des essais". Il a assuré que de nouvelles versions étaient en cours au cas où, tout en espérant ne pas en avoir besoin: "Il faut être préparé".
Variant Afrique du Sud
Les résultats sont moins optimiste pour le variant d'Afrique du Sud. Lors de la conférence de presse de la HAS, le Pr Daniel Floret, a expliqué qu'une étude menée en Afrique du Sud aurait montré une efficacité plus réduite, mais les données restent peu nombreuses. Le scientifique a affirmé qu'il ne pouvait y avoir aucune confirmation encore sur une efficacité ou non du vaccin Astrazeneca contre le variant étant donné le manque d'étude pour l'instant.
Quelques jours plus tard, l'Afrique du Sud a annoncé suspendre l'utilisation du vaccin Astrazeneca dans sa stratégie vaccinale suite à cette étude dont on connait un peu plus de détails. Menée par l'université du Witwatersrand à Johannesburg sur 2000 volontaires âgés de 31 ans en moyenne, la recherche annonce "une protection limitée contre les formes modérées de la Covid-19 liée au variant sud-africain chez les jeunes adultes". Seulement 22% d'efficacité sont rapportées contre les formes modérées et aucune donnée n'est disponible sur les formes graves. Il s'agit de la seule étude sur très peu de personnes avec une fourchette d'âge peu large également plus de recherches doivent être menées.
Toutefois, le 10 février, l'Organisation mondiale de la santé recommande d'utiliser le vaccin de AstraZeneca même dans les pays qui font face à des nouvelles variantes du coronavirus. Suite aux premières données d'essais en Afrique du Sud montrant que le vaccin offrait une "protection minimale", le directeur de la vaccination de l'OMS, le Dr. Katherine O'Bien, a déclaré de son côté que l'étude sud-africaine "n'était pas concluante" et qu'il était "plausible" que le vaccin prévienne encore une maladie grave. "Il n'y a aucune raison de ne pas recommander son utilisation, même dans les pays où la variante est en circulation" a indiqué le Dr. Alejandro Cravioto, le président de Sage, le groupe stratégique consultatif d'experts de l'OMS sur la vaccination, en conférence de presse selon la BBC.
Du côté du laboratoire, une nouvelle forme du vaccin contenant une séquence du variant Sud-Africain serait en préparation par le laboratoire Astrazeneca.
Des contre-indications
Il est n'est pas recommandé chez les personnes ayant une allergie à l'une des substances active ou l'un des excipients présents dans le vaccin.
Liste des effets secondaires
Les plus fréquents | - réaction cutanée au niveau de la zone d'injection (rougeur, ecchymoses, douleur)céphalées- nausées- myalgies- arthralgies- fatigue- malaise- état fébrile- frissons |
Les fréquents | - vomissements- diarrhées- fièvre |
Les moins fréquents | - Lymphadénopathie- Diminution de l’appétit- Etourdissements- Somnolence- Hyperhidrose- Prurit- Eruption cutanée |
Des syndromes grippaux de forte intensité
Dans son bilan de pharmacovigilance hebdomadaire mis en place depuis le début de la vaccination, l'ANSM rapporte que 5693 cas d'effets indésirables (sur plus de 1 430 000 injections) ont été rapportés au 18 mars 2021. "La grande majorité de ces cas concerne des syndromes pseudo-grippaux, souvent de forte intensité (fièvre élevée, courbatures, céphalées)."
Sur la totalité des injections cela représente peu de déclaration d'effets secondaires pour l'ANSM, d'autant qu'ils font partis des effets indésirables connus et jugés peu dangereux. "Néanmoins, ces déclarations de pharmacovigilance constituent un signal potentiel et font l’objet d’une surveillance particulière par les CRPV et l’ANSM au regard notamment de l’intensité de ces effets", explique l'ANSM.
La vaccin Astrazeneca ayant été principalement mis à disposition des soignants de moins de 64 ans, les établissements de santé ont été prévenus et ont désormais pour recommandation d'échelonner les vaccinations de soignants d'un même service pour éviter que tous soient absents en même temps en cas d'effets indésirables.
Un risque de thromboses "rare" mais qui inquiète
Tout comme avec le vaccin Janssen, c'est l'effet secondaire le plus inquiétant s'étant déclaré après le début de la vaccination sur la population. Au mois de mars 2021, plusieurs pays, dont la France, ont suspendu la vaccination anti covid avec le vaccin Astrazeneca à la suite de signalements inquiétants laissant présager un risque de thrombose.
L'Agence européenne du médicament (EMA) a dû revoir l'étude de la balance bénéfice/risque. Après étude elle confirme le lien entre l'apparition de thromboses et le vaccin Astrazeneca. Néanmoins elle considère le vaccin toujours "sûr et efficace", car cela reste un risque "très rare" déclaré sur des dizaines de patients à travers toute l'Europe sur des millions de doses injectées.
Après étude, des chercheurs allemands ont trouvé une cause, qui reste encore à être confirmée, à ces caillots sanguins qui peuvent se déclarer de façon rare chez des patients vaccinés pour la Covid-19. Selon les résultats de ces scientifiques de l'université Goethe à Francfort dirigés par Rolf Marschalek, publiés dans le Financial Times en mai 2021, "Le problème résiderait dans le vecteurs d'adénovirus que les deux vaccins utilisent pour introduire la protéine de Sars-Cov-2 dans le corps".
Pour se développer, l'anti-virus doit être introduit dans les cellules. Des parties de la protéine du virus, lorsqu'elles sont introduites dans le noyau de la cellule, ne se lieraient pas à la membrane qui l'entoure. Ce sont ces extraits de protéines qui s'échappent de la membrane qui seraient responsables thromboses chez certaines personnes en entrainant une réaction immunitaire. (compter un patient sur 100 00 environ).
Cela pourrait expliquer que cet effet secondaire ne se note pas autant avec les vaccins Pfizer et Moderna puisque ces derniers sont des vaccins à ARN Messager, une technique qui ne fait pas passer la protéine dans la cellule en passant par le fameux noyau.
Le chef de cette étude aurait déclaré être en contact avec le laboratoire Johnson&Johnson fabricants du vaccin Janssen à adénovirus afin d'optimiser le sérum pour éviter cette fuite des parties de protéines. Astrazeneca n'aurait pas encore répondu à sa demande.
"La plupart des cas ont été observés chez des femmes âgées de moins de 60 ans dans les deux semaines après injection", déclare l'EMA dans un communiqué du 7 avril 2021.Néanmoins, les données restent encore faibles pour définir des facteurs de risque de type âge, sexe ou antécédents médicaux. Car d'autre cas se sont déclaré à plusieurs tranches d'âge.
Le nombre de cas de thrombose par rapport aux millions de doses injectées reste faibles selon les experts de la police sanitaire européenne qui souligne un vaccin "efficace" qui "sauve des vies".
Au Royaume-Uni, l'Agence britannique de réglementation des médicaments a interdit l'utilisation du vaccin chez les moins de 30 ans après 30 signalements de caillots sanguins (sur un total de 18,1 millions de doses administrées) suite à une vaccination avec Astrazeneca, dont 7 cas mortels chez eux.
De son côté, la France a décidé de reprendre l'utilisation mais en prenant compte des avis d'un peu tout le monde. Dans un soucis de précaution, la HAS, qui valide les autorisations en France a tout de même tenu à rappeler que l'étude de l'EMA portant sur un nombre de signalements sur un risque possible de "coagulation intravasculaire disséminée et de thrombophlébite cérébrale chez les personnes de moins de 55 ans", elle recommandait le vaccin uniquement au-delà de 55 ans, la majorité des prioritaires étant dans cette catégorie d'âge.
En France, sur la totalité des effets secondaires rapportés (5693 au 18 mars), l'ANSM rapporte que 9 cas de thromboses des grosses veines, "atypiques par leur localication (cérébrale, mais également digestive), pouvant être associés à une thrombopénie ou à des troubles de coagulation ont été déclarés, dont 2 décès." Des cas déclarés 8,5 jours en moyenne après la vaccination chez des personnes sans antécédents particuliers. 7 patients de moins de 55 ans et 2 de plus de 55 ans).
Au 7 mai, 30 cas de thrombose veineuse dont 9 décès ont été recensés en France par l'Agence du médicament sur plus de 3 855 000 injections réalisées au 29 avril 2021.
Thrombose : Quels symptômes ? Comment réagir ?
Egalement appelée phlébite, la thrombose veineuse correspond à la formation d'un caillot sanguin. Si cet obstacle se développe dans une veine superficielle, il n'y a généralement pas lieu de s'inquiéter. En revanche, si c'est une veine profonde qui est affectée, le problème est nettement plus sérieux avec un risque d'embolie pulmonaire. Zoom sur ce mécanisme.
"Déclenchement d’une maladie inexpliquée" pendant les essais
Le 8 décembre la revue The Lancet a qualifié le vaccin de "sûr" avec un seul patient sur les 23 754 participants ayant développé "un effet secondaire sérieux possiblement lié".
Le 9 septembre 2020, Astrazeneca avait annoncé avoir suspendu volontairement les essais pour son vaccin candidat dans un communiqué suite au "déclenchement d’une maladie inexpliquée sur l’un des volontaires durant la phase III des essais cliniques". Aucun détail de plus n’a été communiqué par le laboratoire concernant le cas du patient. "Il s’agit d’une étape classique, avait expliqué le laboratoire dans son communiqué. Au cours de grands essais cliniques des effets secondaires se déclarent et nous devons les étudier avec précaution et indépendamment du reste. La sécurité de notre travail étant la priorité".
Trois jours après, le 12 septembre, un nouveau communiqué annonçait la reprise des essais en Grande-Bretagne autorisée par la Medecines Health Regulatory Authority (MHRA), autorité sanitaire anglaise ayant jugé les données de sécurité suffisantes pour poursuivre les tests. Dans un article mis à jour le 17 septembre, le New York Times, explique qu’une source proche du dossier leur aurait révélé qu’il s’agissait d’une une myélite transverse, maladie neurologique rare provoquée par une inflammation touchant la moelle épinière avec affectation des fonctions motrices. Néanmoins, les journalistes américains précisent qu'aucune information ne leur a permis de savoir le timing du diagnostic et s’il était lié au vaccin ou non.
"AstraZeneca et l’université d’Oxford, en tant que commanditaire de l’essai, ne peuvent pas divulguer d’autres informations médicales", a déclaré le laboratoire essuyant des critiques de la communauté médicale pour son manque de transparence quant à l’évaluation du risque détecté. Dans un billet pour le magazine Forbes, William A.Haseltine, médecin et ancien professeur à la Harvard Medical School a regretté que les détails de l’investigation n’aient pas été révélés. : “C’est bien de montrer que les essais sont suspendus pour la sécurité des patients, mais le manque de transparence de la part du laboratoire pharmaceutique appelle à la prudence.”
Après la validation du vaccin sur le marché, Elisabeth Bouvet, membre de la HAS a confirmé deux cas de myélite et un autre de maladie neurologique "de type sclérose en plaques". Une étude par des groupes indépendants auraient confirmé qu'il n'y avait pas de lien avec le vaccin étant donné la présence de lésions antérieures à la vaccination.
Autre réserve : aucun vaccin avec un adénovirus de chimpanzé comme vecteur et non celui d’un adénovirus humain n’a encore été validé. Aucun historique d’étude ne permet de renseigner sur d’éventuels risques pour l’homme.
Un trouble hématologique peu fréquent
Une étude menée sur 5,4 millions de patients par une équipe de médecins en Ecosse a révélé un très faible risque de trouble sanguin appelé purpura thrombocytopénique idiopathique (PTI). En comparant les examens sanguins de personnes ayant reçu une première injection de vaccin Oxford/Astrazeneca avec d'autres personnes non vaccinées, le groupe de chercheurs a identifié un risque légèrement plus élevé de PTI chez 1,7 million de personnes dans le groupe de ceux ayant été vaccinés. Le risque étant principalement chez des personnes souffrant de maladies chroniques (diabète, maladies cardiovasculaires etc.). Leurs résultats publiés dans la revue scientifique Nature Medecin estiment qu'il y aurait 11 cas de PTI pour un millions de doses de vaccin Astrazeneca. Un ratio qui serait semblable au vaccin ROR (rougeole/oreillons/rubéole).
Des cas de syndrome de Guillain-Barré
En Inde, des médecins de l'hôpital de la ville de Kochi, ont remarqué 7 cas de syndrome de Guillain-Barré après l'injection du vaccin d'AstraZeneca. De même en Angleterre dans l'hôpital de Nottingham. Au total, 11 cas ont été signalés (aucun en France). Les symptômes se sont déclarés 11 à 22 jours après la première dose.
Comme l'indique l'OMS, cette pathologie est d'habitude très rare. Lorsqu'un patient est affecté, son système immunitaire attaque une partie du système nerveux périphérique, et peut atteindre les nerfs reliés aux mouvements musculaires. Cela cause une faiblesse musculaire et une perte des sensations au niveau des membres inférieurs et supérieurs.
Pour l'heure, aucun lien de cause à effet n'a été établi entre en le vaccin britannique et le syndrome de Guillain-Barré. Mais certains patients avaient souffert de cette pathologie après avoir eu le Covid-19. "On a déjà eu ce genre de débat avec la grippe et la vaccination antigrippale, indique à Medisite Thomas Kassab, pharmcien. On avait accusé à tort le vaccin antigrippal de développer des syndromes de Guillain-Barré. Or, plusieurs études internationales ont démontré plus tard qu'il y avait moins de Guillain-Barré chez les gens vaccinés contre la grippe que chez ceux qui n'avaient pas reçu le vaccin. Il semblerait que le vaccin n'ait fait que révéler un Guillain Barré sous-jacent, mais ne l'a pas 'créé'."
Le 8 septembre, l'Agence européenne du médicament a recensé 833 cas de syndrome de Guillain Barré dans le monde au 31 juillet 2021 pour plus de 592 millions de doses du vaccin Vaxzevria administrées au 25 juillet 2021. Sur la base de ces données et avec l'appui d'un expert neurologue de l'agence, le Comité d’évaluation des risques en matière de pharmacovigilance de l’EMA (PRAC) juge qu'une "relation causale entre Vaxzevria et le syndrome de Guillain-Barré est considérée au moins comme une possibilité raisonnable et que le syndrome de Guillain-Barré doit donc être ajouté sur les informations de ce vaccin comme un effet secondaire de Vaxzevria". La catégorie de fréquence désigné est "très rare" (soit moins d'une personne sur 10 000).
Comment réagir en cas d'effets secondaires ?
En cas d'effets secondaires fréquents
Si après avoir été vacciné par Astrazeneca vous souffrez d'un des symptômes parmi les plus fréquents (voir la liste complète ci-dessus), comme de la fatigue, des maux de tête, des frissons, des nausées, vomissements, diarrhées etc. L'Agence française du médicament conseille l'utilisation de paracétamol à la dose la plus faible et la moins longtemps possible. Les effets se dissipent généralement "spontanément quelques jours après la vaccination".
En cas de choc anaphylactique
Les réactions allergiques sont peu fréquentes mais possibles. Au moindre signe de réactions cutanées sévère de type gonflement du visage (paupières, lèvres), fortes démangeaisons, problèmes respiratoires, diarrhées, l'ANSM invite à contacter le SAMU (composer le 15). Dans l'attente des secours il faut garder le patient dans une position demi-assise en cas de troubles de la respiration, en décubitus dorsal avec jambes surélevées en cas de malaise conscient et en position latérale de sécurités si la patient est inconscient.
En cas d'effets secondaires rares ou sévères
Si vous êtes victimes d'une réaction non citée dans les effets secondaires fréquents,prenez contact avec un professionnel de santé ou le Samu (en fonction de la gravité)
Concernant les risque de thrombose :si vous avez été vacciné contre la Covid avec Astrazeneca et que vous ressentez des symptômes persistants "quelques jours après la vaccination (au delà de 3 jours) tels que : un essoufflement, une douleur thoracique, un gonflement des jambes, une douleur abdominale, des maux de têtes sévères, une vision floue, ou des ecchymoses à distance du site d’injection", il est conseiller de consulter un médecin immédiatement.
Que faire si j'ai moins de 55 ans et j'ai été vacciné par Astrazeneca ?
Les risques de thromboses chez les moins de 55 ans ayant été identifiés plusieurs semaines après le début de l'utilisation du vaccin dans la campagne vaccinale, plusieurs personnes en dessous de cet âge avaient reçu la première injection du vaccin. En conséquent la HAS a établi, vendredi 9 avril, que les personnes concernées doivent "compléter le schéma vaccinal pour cette population avec un vaccin à ARNm dans un délai de 12 semaines après la première injection." Une dose des vaccin Pfizer/BioNtech (COMIRNATY®)ou Moderna leur sera donc inoculée puisque qu'une seule dose de vaccin ne suffit pas à être totalement protégé.
Diapo : Coronavirus : les bons gestes pour se protéger quand on va faire ses courses
Consulter en ligne un généraliste
Besoin d’un avis médical rapidement ? Prenez rendez-vous simplement avec un généraliste
Consulter ConsulterJ'accepte que Doctissimo utilise mes données de navigation, à savoir ma redirection vers un site de téléconsultation avec un professionnel de santé, uniquement à des fins de mesure d'audience *
Si vous refusez, vous serez redirigé vers le site de téléconsultation sans que Doctissimo n'en ait connaissance. De plus, si vous avez refusé l'utilisation de cookies à des fins de mesure d'audience au travers du module de paramétrage des cookies, aucune mesure d'audience ne sera réalisée quel que soit le choix que vous avez exprimé ici. Pour en savoir plus sur la gestion de vos données personnelles et pour exercer vos droits, vous pouvez consulter notrepolitique de protection des données personnelles.
Je refuse J’accepteLe retard de livraison des doses en France
De nouveaux retards de livraison de doses de vaccins sont à craindre en Europe du côté du groupe Astrazeneca. L'entreprise a annoncé le samedi 13 mars dernier une "des restrictions d'exportations" qui vont entraîner une réduction des livraisons au premier trimestre à cause de difficultés de production. 100 millions de doses étaient attendues au premier trimestre et 70 au deuxième.
Alors que l'autorisation conditionnelle de mise sur le marché par l'Agence du médicament européenne a été donnée comme prévu le 29 janvier, le laboratoire Astrazeneca avait déjà été épinglé après une annonce vendredi 22 janvier à l'AFP d'un retard de livraison en raison "d'une baisse de rendement" dans une usine européenne.
Une annonce qui a immédiatement suscité des inquiétudes de la part des autorités sanitaire Européennes et des états membres alors qu'une nouvelle course contre la montre s'est engagé dans le cadre de la pandémie entre campagne vaccinale et propagation des nouveaux variants anglais, sud-africain, brésilien et maintenant californien. D'autant que des retards ont également été annoncés du côté de Pfizer.
En tout, 400 millions de doses ont été commandées par la Commission Européenne. Le ministre Autrichien de la Santé Rudolf Anschober a déploré sur Twitter un retard avec une conséquence entraînant une livraison en février de 340 000 doses au lieu de 650 000. La commission européenne, peu satisfaite des explications du laboratoire, a fait saisir et demandé l'inspection des données jeudi 28 janvier.
Une pression supplémentaire a été effectuée avec la publication du contratsigné avec le laboratoire en août 2020. On peut y lire que la production est assurée par 2 usines britanniques et 2 européennes et toutes doivent contribuer à l'effort de chacun. Or le Monde rapporte que Pascal Soriot, président directeur général français d'Astrazeneca aurait expliqué devoir garder les doses produites au Royaume-Uni, pour le Royaume-Uni seulement. Des déclarations immédiatement contestées par l'Union Européenne qui réitère que les usines anglaises doivent, elles aussi, participer à l'effort pour l'Europe.